Neirodeģeneratīvas slimības(NDD) raksturo progresējošs vai pastāvīgs specifisku neaizsargātu neironu populāciju zudums smadzenēs vai muguras smadzenēs. NDD klasifikācija var balstīties uz dažādiem kritērijiem, tostarp neirodeģenerācijas anatomisko sadalījumu (piemēram, ekstrapiramidāli traucējumi, frontotemporāla deģenerācija vai spinocerebelāra ataksija), primārām molekulārām anomālijām (piemēram, amiloīds-β, prioni, tau vai α-sinukleīns) vai galvenajām klīniskajām pazīmēm (piemēram, Parkinsona slimība, amiotrofiskā laterālā skleroze un demence). Neskatoties uz šīm atšķirībām klasifikācijā un simptomu izpausmē, tādiem traucējumiem kā Parkinsona slimība (PS), amiotrofiskā laterālā skleroze (ALS) un Alcheimera slimība (AS) ir kopīgi pamatā esošie procesi, kas noved pie neironu disfunkcijas un galu galā šūnu nāves.
Tā kā miljoniem cilvēku visā pasaulē ir cietuši no nesteroīdajām neiroloģiskajām slimībām (NDD), Pasaules Veselības organizācija lēš, ka līdz 2040. gadam šīs slimības kļūs par otro galveno nāves cēloni attīstītajās valstīs. Lai gan ir pieejamas dažādas ārstēšanas metodes, lai mazinātu un pārvaldītu ar konkrētām slimībām saistītos simptomus, efektīvas metodes šo slimību progresēšanas palēnināšanai vai izārstēšanai joprojām nav pieejamas. Jaunākie pētījumi liecina par ārstēšanas paradigmu maiņu no vienkāršas simptomātiskas ārstēšanas uz šūnu aizsargmehānismu izmantošanu, lai novērstu turpmāku pasliktināšanos. Plaši pierādījumi liecina, ka oksidatīvajam stresam un iekaisumam ir izšķiroša nozīme neirodeģenerācijā, pozicionējot šos mehānismus kā kritiskus mērķus šūnu aizsardzībai. Pēdējos gados fundamentālie un klīniskie pētījumi ir atklājuši hiperbariskās skābekļa terapijas (HBOT) potenciālu neirodeģeneratīvo slimību ārstēšanā.
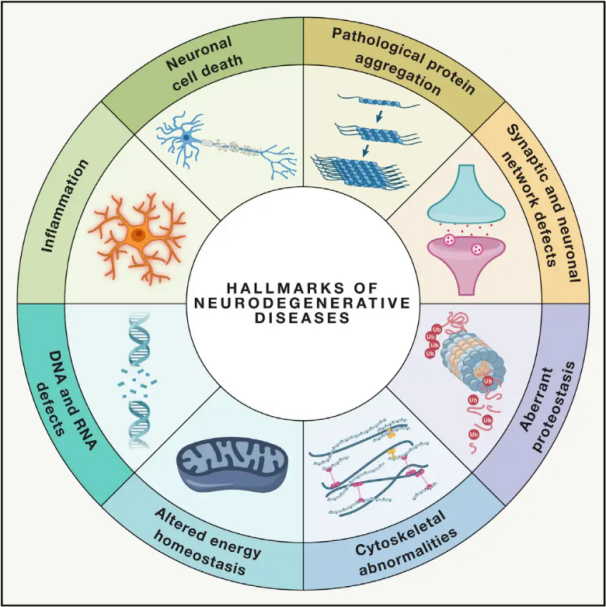
Hiperbariskās skābekļa terapijas (HBOT) izpratne
HBOT parasti ietver spiediena paaugstināšanu virs 1 absolūtās atmosfēras (ATA) — spiediena jūras līmenī — uz 90–120 minūtēm, un bieži vien ir nepieciešamas vairākas sesijas atkarībā no konkrētās ārstējamās slimības. Paaugstinātais gaisa spiediens uzlabo skābekļa piegādi šūnām, kas savukārt stimulē cilmes šūnu proliferāciju un uzlabo dzīšanas procesus, ko mediē noteikti augšanas faktori.
Sākotnēji HBOT pielietojums tika balstīts uz Boila-Mariota likumu, kas postulē spiediena atkarīgu gāzes burbuļu samazināšanos, kā arī augsta skābekļa līmeņa ieguvumus audos. Ir zināms, ka virkne patoloģiju, kurām labvēlīgs ir HBOT radītais hiperoksiskais stāvoklis, tostarp nekrotiski audi, starojuma radīti ievainojumi, traumas, apdegumi, nodalījuma sindroms un gāzes gangrēna, kā arī citas, ko uzskaitījusi Zemūdens un hiperbariskās medicīnas biedrība. Jāatzīmē, ka HBOT ir pierādījis efektivitāti arī kā papildterapijas līdzekli dažādos iekaisuma vai infekcijas slimību modeļos, piemēram, kolītā un sepsē. Ņemot vērā tā pretiekaisuma un oksidatīvos mehānismus, HBOT piedāvā ievērojamu potenciālu kā terapeitisku līdzekli neirodeģeneratīvo slimību ārstēšanā.
Hiperbariskās skābekļa terapijas preklīniskie pētījumi neirodeģeneratīvo slimību gadījumā: ieskatījumi no 3×Tg peles modeļa
Viens no ievērojamākajiem pētījumiemkoncentrējās uz Alcheimera slimības (AS) 3×Tg peļu modeli, kas demonstrēja HBOT terapeitisko potenciālu kognitīvo traucējumu mazināšanā. Pētījumā tika iesaistītas 17 mēnešus vecas 3×Tg peļu tēviņi, salīdzinot ar 14 mēnešus veciem C57BL/6 peļu tēviņiem, kas kalpoja par kontroles grupu. Pētījums parādīja, ka HBOT ne tikai uzlaboja kognitīvās funkcijas, bet arī ievērojami samazināja iekaisumu, plātnīšu daudzumu un Tau fosforilēšanu — kritisku procesu, kas saistīts ar AS patoloģiju.
HBOT aizsargājošā iedarbība tika saistīta ar neiroiekaisuma samazināšanos. To apliecināja mikrogliju proliferācijas, astrogliozes un iekaisumu veicinošu citokīnu sekrēcijas samazināšanās. Šie atklājumi uzsver HBOT divējādo lomu kognitīvo spēju uzlabošanā, vienlaikus mazinot ar Alcheimera slimību saistītos neiroiekaisuma procesus.
Citā preklīniskā modelī tika izmantotas 1-metil-4-fenil-1,2,3,6-tetrahidropiridīna (MPTP) peles, lai novērtētu HBOT aizsargmehānismus attiecībā uz neironu funkciju un motoriskajām spējām. Rezultāti liecināja, ka HBOT veicināja uzlabotu motorisko aktivitāti un satvēriena spēku šīm pelēm, korelējot ar mitohondriju bioģenēzes signalizācijas palielināšanos, īpaši aktivizējot SIRT-1, PGC-1α un TFAM. Tas uzsver mitohondriju funkcijas nozīmīgo lomu HBOT neiroprotektīvajā iedarbībā.
HBOT mehānismi neirodeģeneratīvās slimībās
HBOT izmantošanas pamatprincips neirodeģeneratīvo slimību (NDD) gadījumā ir saistība starp samazinātu skābekļa piegādi un uzņēmību pret neirodeģeneratīvām izmaiņām. Hipoksijas inducējamais faktors-1 (HIF-1) spēlē centrālu lomu kā transkripcijas faktors, kas nodrošina šūnu adaptāciju zemam skābekļa spiedienam, un ir iesaistīts dažādās NDD, tostarp AD, PD, Hantingtona slimības un ALS, atzīmējot to kā svarīgu zāļu mērķi.
Tā kā vecums ir nozīmīgs vairāku neirodeģeneratīvu slimību riska faktors, ir svarīgi izpētīt HBOT ietekmi uz novecošanās neirobioloģiju. Pētījumi liecina, ka HBOT var uzlabot ar vecumu saistītus kognitīvos traucējumus veseliem gados vecākiem cilvēkiem.Turklāt gados vecākiem pacientiem ar ievērojamiem atmiņas traucējumiem pēc HBOT iedarbības bija novērojami kognitīvie uzlabojumi un palielināta smadzeņu asins plūsma.
1. HBOT ietekme uz iekaisumu un oksidatīvo stresu
HBOT ir pierādījusi spēju mazināt neiroiekaisumu pacientiem ar smagu smadzeņu disfunkciju. Tam piemīt spēja samazināt iekaisuma citokīnu (piemēram, IL-1β, IL-12, TNFα un IFNγ) līmeni, vienlaikus palielinot pretiekaisuma citokīnu (piemēram, IL-10) līmeni. Daži pētnieki ierosina, ka HBOT radītās reaktīvās skābekļa sugas (ROS) ietekmē vairākus terapijas labvēlīgus efektus. Līdz ar to, papildus spiediena atkarīgajai burbuļu mazināšanas iedarbībai un augsta audu skābekļa piesātinājuma sasniegšanai, ar HBOT saistītie pozitīvie rezultāti daļēji ir atkarīgi no radīto ROS fizioloģiskajām lomām.
2. HBOT ietekme uz apoptozi un neiroprotekciju
Pētījumi liecina, ka HBOT var samazināt p38 mitogēna aktivētās proteīna kināzes (MAPK) hipokampālā fosforilēšanu, tādējādi uzlabojot izziņu un mazinot hipokampa bojājumus. Ir konstatēts, ka gan atsevišķs HBOT, gan kombinācijā ar Ginkgo biloba ekstraktu samazina Bax ekspresiju un kaspāzes-9/3 aktivitāti, kā rezultātā samazinās aβ25-35 inducētās apoptozes ātrums grauzēju modeļos. Turklāt citā pētījumā tika pierādīts, ka HBOT iepriekšēja kondicionēšana izraisīja toleranci pret smadzeņu išēmiju, un mehānismi ietver palielinātu SIRT1 ekspresiju, kā arī palielinātu B šūnu limfomas 2 (Bcl-2) līmeni un samazinātu aktīvās kaspāzes-3 līmeni, uzsverot HBOT neiroprotektīvās un antiapoptotiskās īpašības.
3. HBOT ietekme uz asinsriti unNeiroģenēze
HBOT iedarbība uz galvaskausa asinsvadu sistēmu ir saistīta ar vairākkārtēju ietekmi, tostarp hematoencefāliskā barjeras caurlaidības uzlabošanos, angioģenēzes veicināšanu un tūskas mazināšanu. Papildus palielinātai skābekļa piegādei audiem, HBOTveicina asinsvadu veidošanosaktivizējot transkripcijas faktorus, piemēram, asinsvadu endotēlija augšanas faktoru, un stimulējot neironu cilmes šūnu proliferāciju.
4. HBOT epiģenētiskā ietekme
Pētījumi ir atklājuši, ka cilvēka mikrovaskulāro endotēlija šūnu (HMEC-1) pakļaušana hiperbariskajam skābeklim būtiski regulē 8101 gēnu, tostarp gan augšupregulētu, gan lejupregulētu ekspresiju, izceļot gēnu ekspresijas pieaugumu, kas saistīts ar antioksidantu atbildes ceļiem.
Secinājums
HBOT lietošana laika gaitā ir ievērojami uzlabojusies, pierādot tā pieejamību, uzticamību un drošību klīniskajā praksē. Lai gan HBOT ir pētīta kā neinvazīva ārstēšanas metode NDD ārstēšanai, un ir veikti daži pētījumi, joprojām ir steidzami nepieciešami stingri pētījumi, lai standartizētu HBOT praksi šo slimību ārstēšanā. Ir svarīgi turpināt pētījumus, lai noteiktu optimālo ārstēšanas biežumu un novērtētu labvēlīgās ietekmes apmēru pacientiem.
Rezumējot, hiperbariskā skābekļa un neirodeģeneratīvo slimību krustošanās liecina par daudzsološu terapeitisko iespēju robežu, kas attaisno turpmāku izpēti un validāciju klīniskajos apstākļos.
Publicēšanas laiks: 2025. gada 16. maijs

